【IBS】便秘型肠易激综合征克星—利那洛肽
推行健康生活方式、实现全民健康是实现《‘健康中国2030’规划纲要》的重要一环。肠道健康与我们的身体健康息息相关,但很容易被忽视。肠易激综合征(IBS)是消化科常见的胃肠功能性疾病之一,症状易反复发作,严重影响患者的生活质量,其亚型之一的便秘型IBS(IBS-C),临床表现以慢性便秘、腹痛、腹胀为主,传统的治疗方案无法同时满足改善腹痛、腹胀及便秘的治疗目标,且存在耐药,不良反应等局限性。
利那洛肽是一款可显著缓解IBS-C患者便秘及腹痛、腹胀等症状的多肽药物,且具有良好的安全性。因此,利那洛肽成为了IBS-C应用的新选择。

01
关于利那洛肽
利那洛肽是什么
利那洛肽是由美国Ironwood公司研发的一种鸟苷酸环化酶 C(GC-C) 激动剂,于2012 年 8 月 30 日获美国 FDA 批准上市,商品名为 Linzess。美国FDA批准将利那洛肽用于治疗慢性特发性便秘和便秘型肠易激综合征(IBS-C)。临床研究证明,利那洛肽能显著改善慢性便秘和IBS-C患者的便秘、腹痛、腹胀等症状。利那洛肽耐受性良好,严重不良事件罕见,最常见的不良反应为轻、中度腹泻。因此,对于慢性便秘和IBS-C的患者,利那洛肽是非常有前景的治疗药物。
利那洛肽结构及作用机制[1]
利那洛肽是鸟苷肽家族的第一类14个氨基酸肽,含有3对二硫键,是肠上皮细胞管腔表面鸟苷酸环化酶-c (GC-C)受体的选择性激动剂。GC-C(鸟苷肽激素,鸟苷和鸟苷)的内源性配体与受体结合,促进肠道分泌物对膳食的反应。通过鸟苷肽(包括利那洛肽)激活GC-C,导致环鸟苷(cGMP)水平升高,这是在肠液的调节和分泌中起关键作用的第二信使。
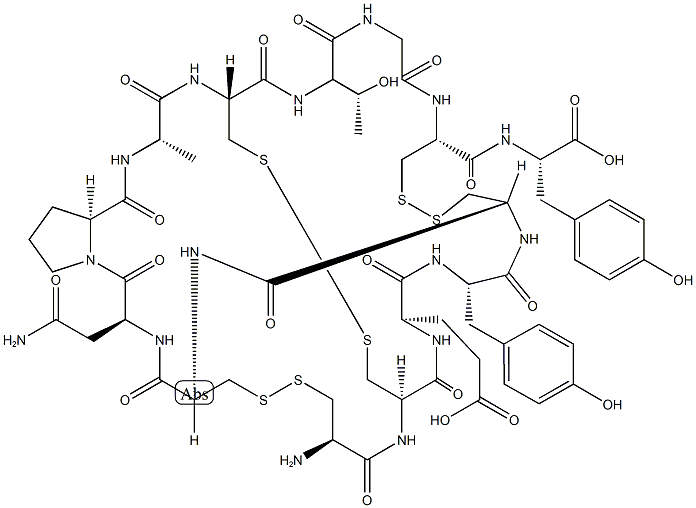
利那洛肽结构示意图
细胞内cGMP的升高触发了cGMP蛋白激酶的激活和随后下游靶点的磷酸化,包括囊性纤维化跨膜电导调节(CFTR)离子通道。CFTR通道的激活导致氯离子和碳酸氢盐离子进入肠腔的分泌增加,最终导致肠液分泌增加和胃肠道运输加快。
在内脏过敏的啮齿动物模型中,利那洛肽能减轻肠道疼痛,可能是由于GC-C激活介导的传入疼痛纤维脱敏的结果。因此,GC-C正在成为IBS-C和CIC治疗的治疗靶点,因为它具有加速胃肠道转运和减少腹痛的双重作用。
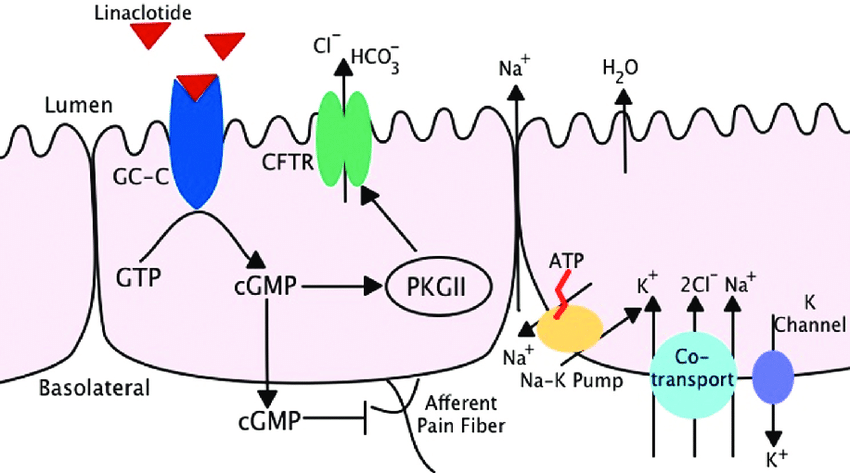
利那洛肽的作用机理
利那洛肽市场应用
截至目前,令泽舒(Linzess)已获美国FDA批准3种剂量:290微克用于便秘型肠易激综合征(IBS-C)成人患者的治疗,145微克和72微克用于慢性特发性便秘(CIC)成人患者的治疗。
利那洛肽在美国等全球30多个国家获批上市。目前,利那洛肽已成为全球治疗便秘型肠易激综合征的领先处方药。在美国,linaclotide品牌名为Linzess,由Ironwood与艾尔健(Allergan)联合营销。在欧洲,linaclotide品牌名为Constella,由艾尔健负责营销,目前艾尔健于2020年5月8日被艾伯维(AbbVie)收购。在日本,安斯泰来于2009年与Ironwood签署授权协议,负责在日本市场的开发及商业化。
在中国,阿斯利康于2012年与Ironwood达成合作,共同负责linaclotide在中国(包括香港、澳门)的开发及商业化[2]。
02
利那洛肽的临床应用
利那洛肽在慢性便秘患者中的应用
研究表明利那洛肽治疗慢性便秘安全、有效,2011年The New England Journal of Medicine上发表了2项Ⅲ期临床试验(试验303和试验01)[3]。该2项研究共纳入北美212个治疗中心的1 276例慢性便秘患者,分别随机给予145、290 μg/d利那洛肽和安慰剂治疗。主要疗效终点为在12周治疗期内,至少9周完全自发排便(complete spontaneous bowel movement,CSBM)≥3次/周,且比基线增加≥1次。次要终点包括每周排便次数、粪便稠度、腹部不适、腹胀和便秘严重程度。结果表明2项研究的145 μg/d治疗组分别有21.2%和16.0%、290 μg/d治疗组分别有19.4%和21.3%的患者达到了主要疗效终点,安慰剂组分别有3.3%和6.0%的患者达到了主要疗效终点。关于2项研究中所有次要终点的改善程度,利那洛肽组均显著优于安慰剂组。以上比较,差异均有统计学意义(P均<0.01)。
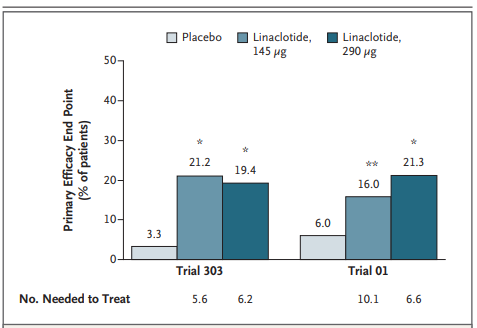
每个试验中利那洛肽组和安慰剂组的主要疗效终点
在慢性便秘相关腹部症状中,腹胀和腹痛一直是治疗的难点。一项Ⅲ期事后汇总分析比较了伴轻度腹痛CIC患者和伴中度至重度腹痛CIC患者在利那洛肽治疗后的症状改善情况,共纳入1 271例CIC患者,在治疗前2周至治疗12周期间每天评估患者的腹部和肠道症状[4]。结果显示,在接受2个不同剂量的利那洛肽治疗时,轻度腹痛亚组和中重度腹痛亚组患者的腹痛、腹部不适和腹胀评分均较基线水平显著改善,中重度亚组的变化大于轻度亚组的变化,差异均有统计学意义(P均<0.05)。
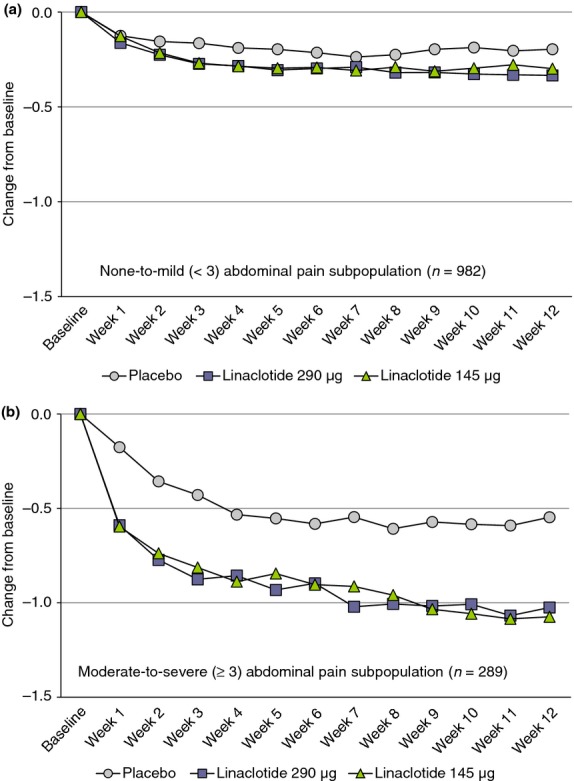
腹痛周平均变化
2015年发表的1项纳入483例CIC伴中重度腹胀患者的Ⅲ期研究,再次证实了利那洛肽(145 μg和290 μg)对CIC患者腹胀症状的改善效果[5]。与安慰剂相比,2种剂量的利那洛肽治疗均可显著改善CIC患者的中度至重度腹胀症状,差异均有统计学意义(P均<0.05)。因此,利那洛肽不仅可以改善慢性便秘患者的便秘症状,对伴有腹胀、腹部不适患者的治疗也具有重要意义。
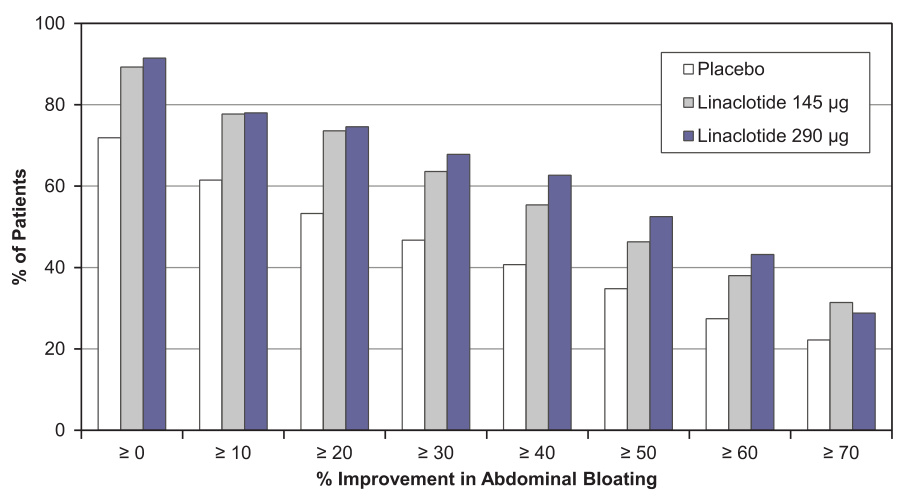
第12周腹胀改善百分比递增
利那洛肽在IBS-C患者中的应用
超过80%的IBS患者在初次就诊期间已接受某种形式的治疗,其中74%服用过至少3种药物,而只有1/3的患者表示对目前疗法满意。利那洛肽已被美国胃肠病协会、美国胃肠病学院以高证据等级、强烈推荐用于治疗IBS-C。3项大型Ⅲ期随机对照试验提供了利那洛肽治疗IBS-C的强有力证据。
Rao等[6]的第1项研究纳入北美118个中心的800例IBS-C患者,将所有患者随机分为安慰剂组和利那洛肽组(290 μg口服,1次/d,治疗持续12周),随后进行为期4周的随机撤药。主要终点采用美国FDA设定的IBS-C有效性评估终点,即12周治疗期间至少6周满足下列2条标准:①每天腹痛最剧烈时疼痛评分较基线下降>30%; ②同一周CSBM较基线增加≥1次。结果显示,利那洛肽组和安慰剂组的主要终点达成率分别为33.6%和21.0%(P<0.01)。利那洛肽缓解便秘症状起效迅速,服药1 d内即出现自发排便,1周内达到最大肠道功能改善;腹痛改善约在1周内起效,6~8周达到最大疗效。最常出现的不良事件是腹泻,导致5.7%的利那洛肽组患者和0.3%的安慰剂组患者停止治疗。
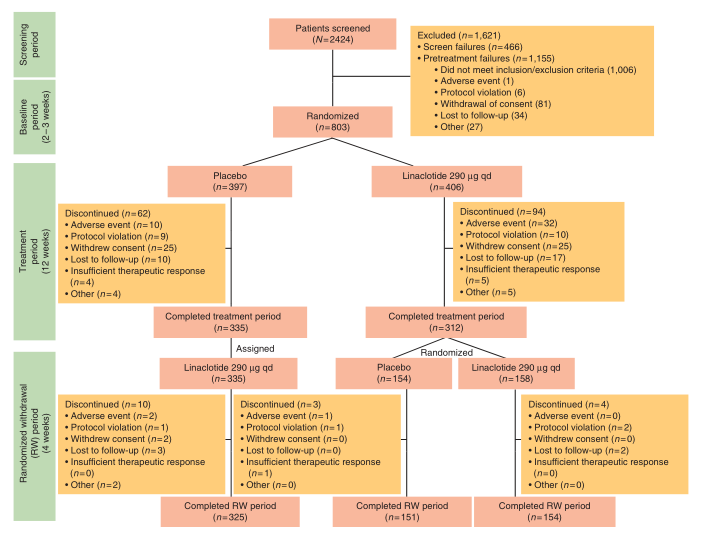
实验人群实验进展流程图
Chey等[7]的第2项研究纳入804例患者,探讨了利那洛肽更长期(26周)治疗对IBS-C患者的有效性和安全性,主要终点依然采用FDA复合终点。利那洛肽组和安慰剂组治疗26周FDA复合终点应答率分别为33.7%和13.9%,腹痛应答率分别为48.9%和34.5%,CSBM应答率分别为47.6%和22.6%,差异均有统计学意义(P均<0.01)。在利那洛肽治疗组,75%的患者腹部症状得到改善,88%的患者每周自发排便次数显著增加,76%的患者每周自主排便增加≥1次,54%的患者每周自主排便增加≥3次。
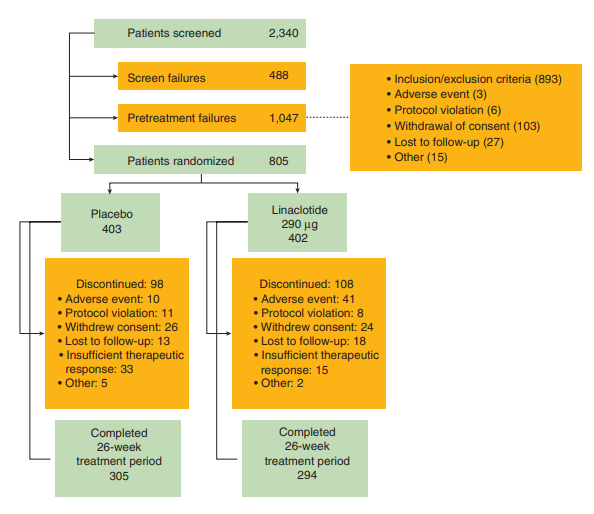
实验人群实验进展流程图
第3项研究[8]主要在中国患者中进行的Ⅲ期临床试验评估了利那洛肽治疗中国IBS-C患者的有效性和安全性。该研究共纳入中国和其他地区的IBS-C患者839例,其中中国患者659例(78.5%)。所有患者按1∶1比例随机接受290 μg利那洛肽或安慰剂治疗12周。利那洛肽组有60.0%(250/417)患者的腹痛、腹部不适症状明显缓解,而安慰剂组为48.8%(206/422),差异有统计学意义(P=0.001)。利那洛肽组患者的IBS症状缓解率为31.7%,显著优于安慰剂组的15.4%(P<0.01)。
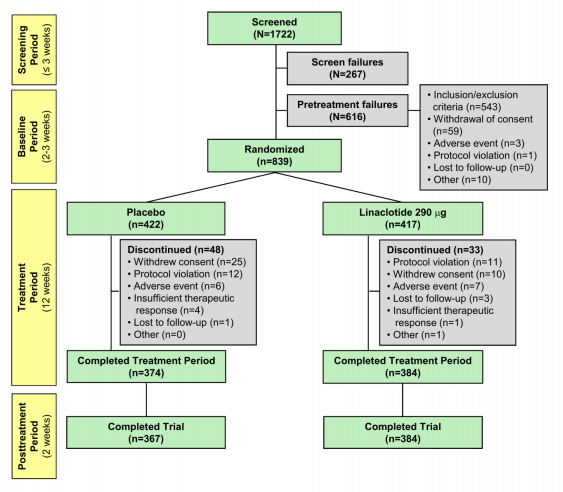
实验人群实验进展流程图
03
利那洛肽未来市场前景
市场新星——利那洛肽
利那洛肽是Ironwood公司推出的治疗便秘的多肽药物。该产品在2012年一经推出,其销售额就节节攀升,2014-2020年年复合增长率达到32.2%,远高于其他同类别治疗便秘的药物。据汤森路透Newport数据统计,2020年全球销售额9.31亿美元,2021年全球销售额高达10.06亿美元,同比增加了8.0%,此外,根据IQVIA数据显示,2021年全年LINZESS胶囊处方总需求为1.59亿粒,比2020年全年增长12%。随着人们对肠易激综合征(IBS)及慢性便秘的用药市场需求不断增加,可以预测利那洛肽未来几年的市场前景也将非常乐观。
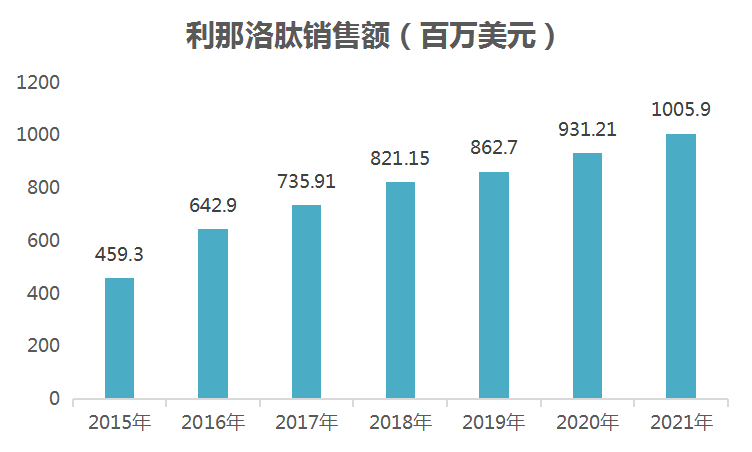
数据来源:Ironwood公司官网
就地域上而言,新型便秘药市场主要集中在美国,但中国具有庞大的患者群,而且发病率日益增加,市场潜力也非常大。据米内网数据显示[9],利那洛肽胶囊进入国内市场后,在中国公立医疗机构终端的销售突飞猛进,2020年增速达41100%,2021上半年也保持在973%的水平。从渠道来看,销售主力依然在城市公立医院,但正逐渐向城市社区中心、乡镇卫生院下沉。在中国城市实体药店终端,2021年预计治疗便秘的药物TOP10产品合计市场份额高达98%,市场集中度极高。阿斯利康的利那洛肽胶囊排在产品TOP7位置,市场份额从2019年的0.24%上涨至2021年约占1.79%,增速依然强劲。据了解,目前主流制剂利那洛肽胶囊(290μg)的价格为350元/7粒,IBS-C患者可以通过医保报销,以低价格享受到优质创新药物。
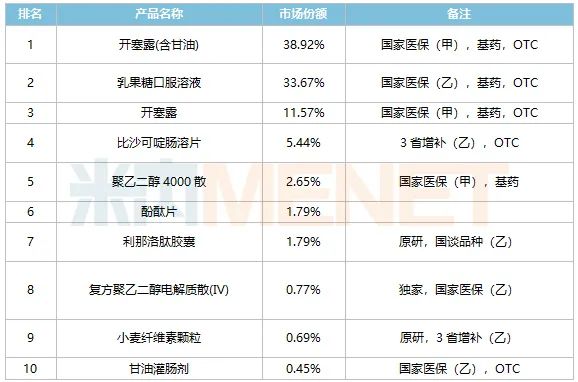
2021E零售市场治疗便秘的药物TOP10产品
(来源:米内网中国城市实体药店终端格局)
展望
慢性便秘和IBS-C均为严重影响患者生命质量的疾病。利那洛肽属于GC-C受体激动剂中的首个创新药物,已在全球广泛用于慢性便秘和IBS-C的治疗。截至目前,大量临床研究表明利那洛肽可有效改善慢性便秘和IBS-C患者的便秘和腹部症状,患者治疗满意度高。III期临床研究结果也证实了利那洛肽在以中国人群为主的IBS-C患者中的有效性和安全性,为中国临床医师带来全新和有效的IBS-C治疗选择[10]。
总之,利那洛肽在便秘治疗领域很有应用前景。期待未来有更多利那洛肽的不同应用方案(如联合用药、最佳给药剂量、最佳给药时间等),且具有良好的疗效和安全性、更具成本效益,真正满足广大患者的临床需求,让患者享受无胀痛,‘便’轻松的生活。

04
湃肽 高技术壁垒的多肽合成研发平台
浙江湃肽生物股份有限公司是一家致力于多肽产业化的国家高新技术企业,拥有全球领先的全固相合成多肽生产与开发工艺,专注于高技术壁垒的多肽原料药研发及生产;拥有超强研发技术团队,已成功研制多个多肽原料药,攻克了在合成端的技术壁垒和价格壁垒。凭借在多肽领域的研发优势、过硬产品质量,获得国内、国际市场较高认可。同时,湃肽一直坚持匠心筑梦,品质为先,力争打造中国多肽领导品牌,持续为客户提供更优质的产品和更专业的服务。

目前公司可批量公斤级生产利那洛肽,制得的利那洛肽精肽纯度高、杂质含量低,最大单杂0.1%。此外,湃肽具备丰富的多肽合成和生产经验,拥有自己的方法数据库,能更快的响应客户的需求,为您生产出最优质的多肽产品。
利那洛肽作为治疗功能性便秘的一线用药之一,在便秘治疗领域具有广阔的市场前景。随着近年来利那洛肽市场的不断扩大,加码布局企业的持续增多,该领域的竞争预计也将逐渐加剧。未来,湃肽将抓住行业发展机遇,聚焦多肽全产业链布局,始终以多肽药物为基础和核心,逐步形成在便秘、肿瘤和糖尿病等多个治疗领域的产品战略布局。
参考文献:
[1]Rachel Hutchins Thomas,PharmD,MS and Kyle Allmond.Linaclotide (Linzess) for Irritable Bowel syndrome With Constipation and For Chronic Idiopathic Constipation.Journal List & P T 2013 Mar,38(3): 154-160.
[2]生物谷.Ironwood缓释剂型Linzess(linaclotide)显著改善便秘型肠易激综合征(IBS-C)患者腹痛症状.
[3]Anthony J Lembo,Harvey A Schneier,Steven J Shiff,et al.Two randomized trials of linaclotide for chronic constipation.N Engl J Med 2011 Aug 11,365(6):527-36.
[4]L Chang,A J Lembo,B J Lavins,,et al.The impact of abdominal pain on global measures in patients with chronic idiopathic constipation, before and after treatment with linaclotide: a pooled analysis of two randomised, double-blind, placebo-controlled, phase 3 trials.Aliment Pharmacol Ther 2014 Dec,40(11-12):1302-12.
[5]Brian E Lacy,Ron Schey,Steven J Shiff,et al.Linaclotide in Chronic Idiopathic Constipation Patients with Moderate to Severe Abdominal Bloating: A Randomized, Controlled Trial.PLoS One 2015 Jul 29,10(7):e0134349.
[6]Satish Rao,Anthony J Lembo,Steven J Shiff,et al.A 12-week, randomized, controlled trial with a 4-week randomized withdrawal period to evaluate the efficacy and safety of linaclotide in irritable bowel syndrome with constipation.Am J Gastroenterol 2012 Nov,107(11):1714-24.
[7]William D Chey,Anthony J Lembo,Bernard J Lavins,et al.Linaclotide for irritable bowel syndrome with constipation: a 26-week, randomized, double-blind, placebo-controlled trial to evaluate efficacy and safety.Am J Gastroenterol 2012 Nov,107(11):1702-12.
[8]Yunsheng Yang,Jingyuan Fang,Xiaozhong Guo,et al.Linaclotide in irritable bowel syndrome with constipation: A Phase 3 randomized trial in China and other regions.J Gastroenterol Hepatol 2018 May,33(5):980-989.
[9] 米内网.【最新】大涨973%!四川药企抢阿斯利康便秘药首仿.
[10]邹多武.利那洛肽:慢性便秘和便秘型肠易激综合征的新选择.中华消化杂志 2019 Apr,39(4):286-288.

扫码关注我们
解锁更多资讯