【行研】降糖新星利拉鲁肽的应用机制探索
上一篇我们围绕胰高糖素样肽-1受体激动剂(GLP-1RA)——索马鲁肽(点击查看原文),介绍了索马鲁肽的应用机制及市场未来应用前景,今天我们将展示索马鲁肽的“孪生兄弟”——利拉鲁肽。作为全球第一款长效GLP-1受体激动剂,利拉鲁肽不仅降糖效果好,而且兼具减重降压、改善血脂谱等显著优势,在GLP-1领域中一举成为“降糖新星”。
1
关于利拉鲁肽
利拉鲁肽是什么
利拉鲁肽(Liraglutide),商品名为Victoza®(诺和力®),为Novo Nordisk公司开发的一种长效GLP-1类似物。该药物可通过促进胰岛素的合成和分泌,抑制胰高糖素分泌,刺激β细胞增殖及新生并抑制β细胞凋亡,促进心肌、骨骼肌和脂肪细胞的葡萄糖摄入,增加肝脏糖原贮积等发挥其高效控糖作用,此外,利拉鲁肽还可延缓胃排空、减少摄食,减轻患者体重,改善血脂和血压控制,同时具有神经和心肌细胞保护作用。
利拉鲁肽结构及作用机制
利拉鲁肽与天然GLP-1有97%的内同源性。与天然的GLP-1相比,利拉鲁肽的分子结构变化是天然的GLP-1第34位赖氨酸残基上被精氨酸取代,第26位赖氨酸残基上增加一个由谷氨酸介导的16碳棕榈酰脂肪酸侧链。利拉鲁肽在保留天然GLP-1所有生物活性的同时,延长了其酰化产物与蛋白结合的时间,可以抵抗二肽酰基肽酶IV (DPP-IV)和中性内肽酶降解作用,从而克服了天然GLP-1易被降解的缺点。同时,利拉鲁肽可以与血液中的白蛋白结合,使其半衰期长达11~13h,适合临床应用,该药分别于2009年6月和2010年1月被欧洲药品评价署(EMEA)和美国食品与药物管理局(FDA)批准上市用于成年人2型糖尿病的治疗。
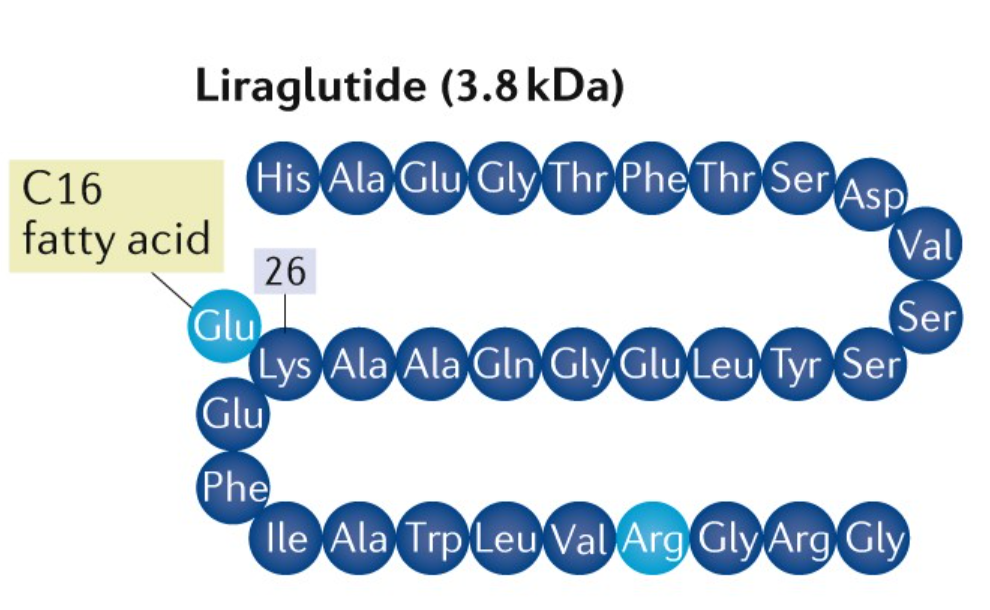
利拉鲁肽结构示意图[1]
利拉鲁肽上市过程
1
2009年,利拉鲁肽率先在欧洲上市。
2
2010年1月25日,美国食品与药物管理局(FDA)批准利拉鲁肽在美国上市,用于Ⅱ型糖尿病治疗,并于2014年12月将利拉鲁肽治疗领域扩大到肥胖症治疗,推出利拉鲁肽减肥针剂Saxenda,使其成为第一款被批准用于减肥的GLP-1类似物。
3
2011年4月13日,获国家食品药品监督管理局批准,用于治疗成人Ⅱ型糖尿病。
4
2011 年,利拉鲁肽以诺和力为商品名获批进入了中国市场。
5
2017年,FDA继续批准了利拉鲁肽用于降低2型糖尿病患者心脏病发作、卒中及心血管死亡风险;同年,利拉鲁肽进入国家医保目录。
6
2019年6月,FDA又批准扩展适应症,用于治疗10岁以上的2型糖尿病患者。
7
2020年5月14日,国家药品监督管理局(NMPA)批准了利拉鲁肽注射液(诺和力®)心血管适应症上市申请。
8
2021年10月28日,NMPA 批准德谷胰岛素利拉鲁肽注射液Xultophy(诺和益® )上市,这是国内首款获批上市的长效胰岛素/GLP-1 复方制剂。
9
Novo Nordisk利拉鲁肽纯化和制剂的专利将于2024年11月17日到期。
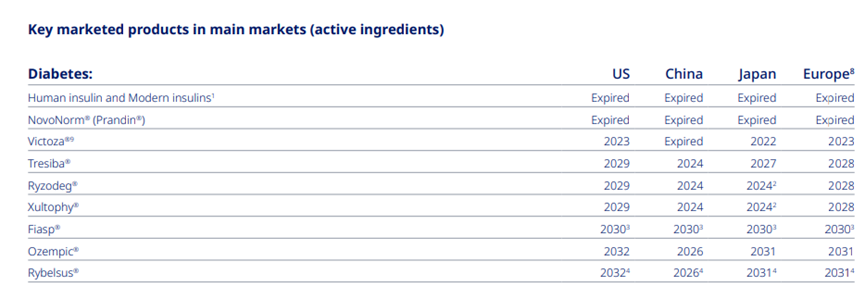
Novo Nordisk重点市场专利状态
(来源:Novo Nordisk 2021公开财报)
利拉鲁肽专利情况
利拉鲁肽吸引众多企业关注,除巨大的销售市场外,另一重要因素是:专利期限。
Novo Nordisk申请的中国专利CN97198413.1是US6268343在中国的同族专利,保护了包括利拉鲁肽在内的GLP-1类似物,将于2017年8月21日失效。Novo Nordisk还就该专利申请了两件分案,且均获授权,专利号分别为CN200510107588.1与CN200610110898.3。以上化合物专利均于2017年过期。然而时至今日,却仍然没有国产利拉鲁肽上市。
Novo Nordisk公司申报的中国专利CN200480034152.8保护了含有利拉鲁肽与丙二醇的制剂,该专利已获授权,将于2024年11月17日失效。两件分案申请一件被驳回,另一件尚在审质审查阶段。
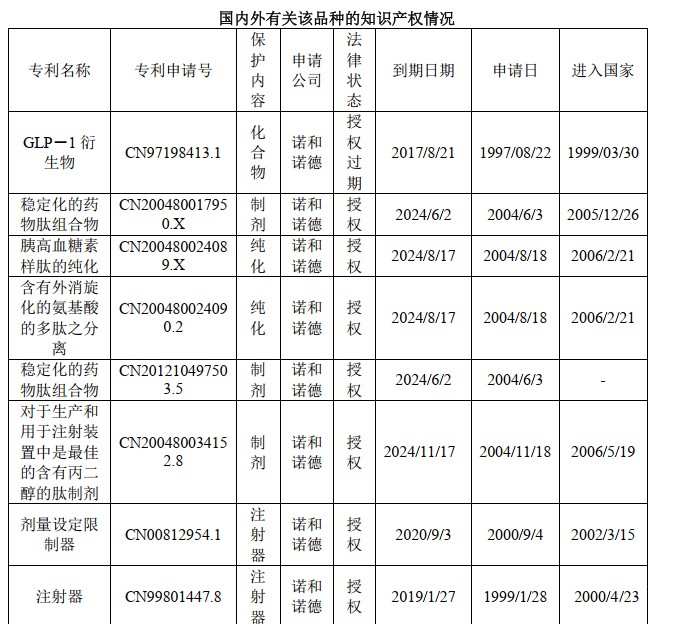
国内外有关该品种的知识产权情况[7]
换言之,利拉鲁肽的仿制药一旦在国内获批上市,价格将冲击原研、抢食市场份额,喝上专利期满的头啖汤。
就目前情况,价格和高技术壁垒是阻碍利拉鲁肽在糖尿病市场发展的两大重要因素,但随着品种专利的陆续到期,国内药品制备工艺的不断提升,医保准入带来的高销量优势,该品种在国内将有更大的发力空间。
2
利拉鲁肽应用机制
治疗2型糖尿病
利拉鲁肽商品名为诺和力®,为预填充注射笔,规格为3mL:18mg。
2011年由杨文英教授领导的在中国口服降糖药物治疗血糖控制不佳的T2DM患者中进行的3期临床研究公布结果。本研究比较了利拉鲁肽0.6mg、1.2mg及1.8mg每日一次联合二甲双胍与格列美脲4mg每日一次联合二甲双胍的疗效和安全性。结果显示经过16周治疗,利拉鲁肽1.2mg、1.8mg降低HbA1c、空腹血糖非劣于格列美脲,利拉鲁肽1.8mg每日一次降低餐后血糖显著优于格列美脲。同时,利拉鲁肽各组低血糖发生率均极低,体现了“智能降糖”的特点。利拉鲁肽治疗显著减轻患者体重,1.8mg利拉鲁肽治疗16周使患者平均减重2.44kg,且减重作用与基线体重指数(BMI)无关。此项研究首次在中国患者中观察了利拉鲁肽的疗效及安全性,基于此,利拉鲁肽在中国成功上市。
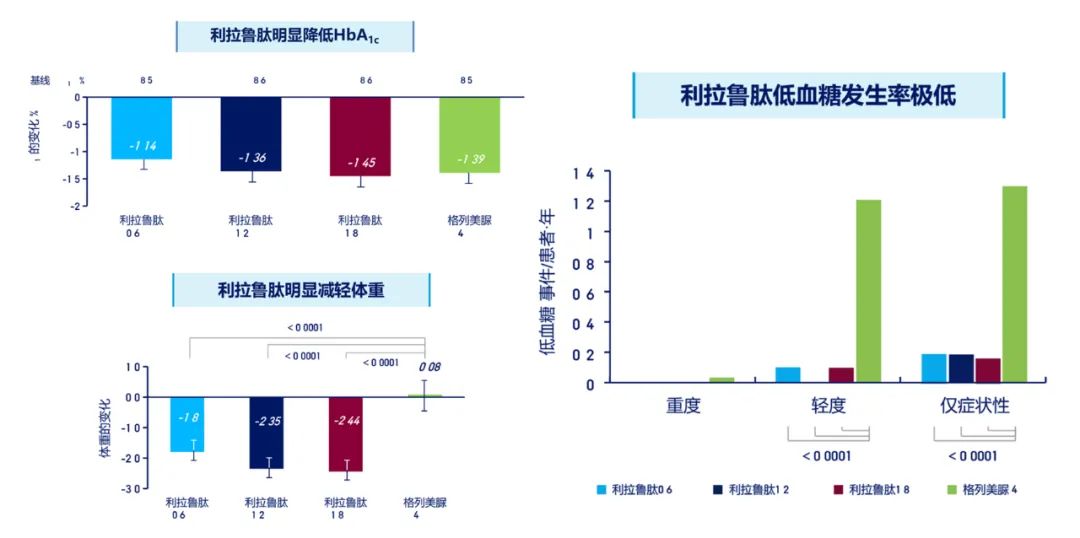
中国上市研究显示利拉鲁肽智能降糖,低血糖风险低[2]
治疗心血管疾病
2017年8月25日,美国食品药品监督管理局(FDA)已批准利拉鲁肽这项降糖之外的适应证,即用于降低伴有心血管疾病的2型糖尿病患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死、非致死性脑卒中)风险。利拉鲁肽这项新适应证的获批,有赖于具有里程碑意义的LEADER研究提供的坚实证据[3]。
LEADER研究为一项国际多中心、随机、双盲、安慰剂对照试验,纳入来自全球32个国家的9340例合并心血管高风险的2型糖尿病患者,评估在标准降糖治疗基础上应用利拉鲁肽1.8mg(或最大耐受剂量)的长期疗效。

LEADER研究
中位随访3.8年时的结果显示,与安慰剂组相比,利拉鲁肽组主要心血管不良事件(心血管死亡、非致死性心肌梗死和非致死性脑卒中)的相对风险降低13%,绝对风险降低1.9%;心血管死亡的相对风险降低22%,全因死亡的相对风险降低15%。
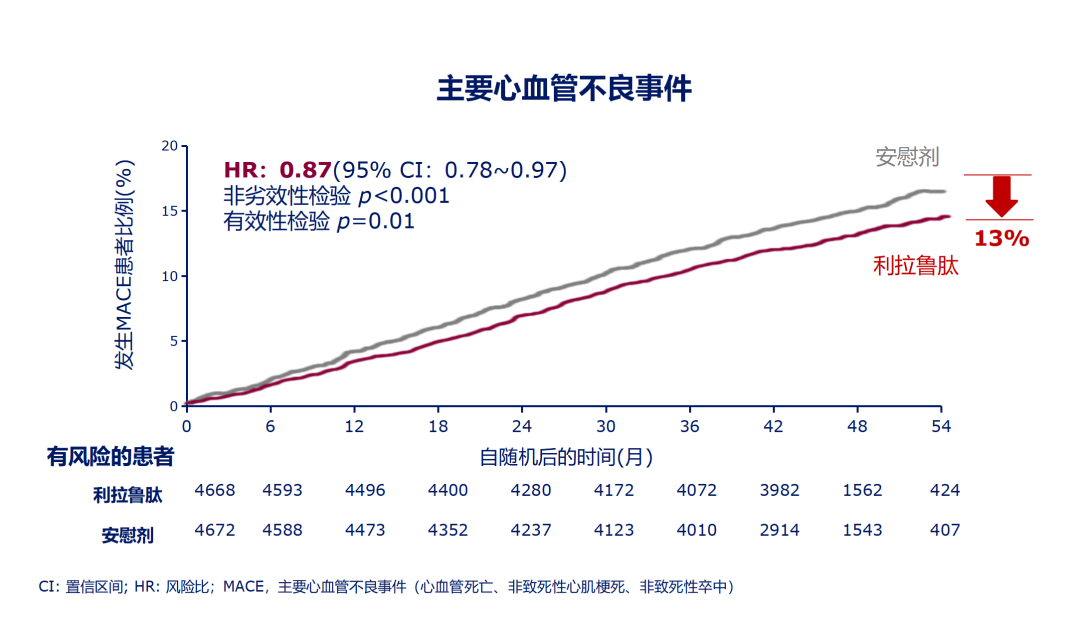
LEADER研究中利拉鲁肽组和安慰剂组主要终点(心血管死亡、非致死性心肌梗死、非致死性脑卒中)发生风险比较
LEADER研究是第一项证实GLP-1受体激动剂(GLP-1RA)可带来心血管获益的CVOT,为近年来心血管和糖尿病指南重要更新提供了有力证据。
*CVOT:心血管结局研究
治疗肥胖
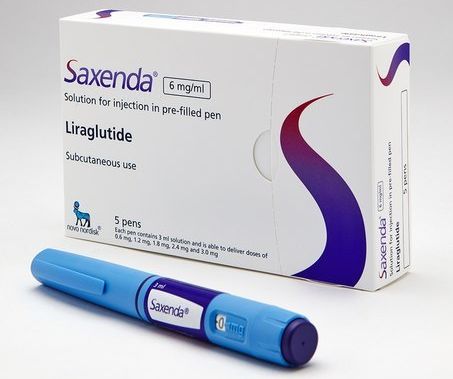
Saxenda(3.0mg注射液)是首个开发用于体重管理的胰高血糖素样肽-1(GLP-1)受体激动剂,于2014年12月获得美国FDA批准:作为低热量饮食和加强运动的辅助手段,用于肥胖(BMI≥30kg/m2)、或超重(BMI≥27kg/m2)且伴有至少一种与体重相关并发症的成人患者,用于长期体重管理。
Saxenda治疗青少年肥胖症的安全性和有效性得到了《新英格兰医学杂志》(NEJM)今年早些时候发表的3a期临床试验数据的支持。这项为期56周的临床试验在251例12-17岁肥胖症患者中开展,研究了Saxenda与安慰剂作为生活方式治疗(定义为:通过健康营养和体育活动进行减肥)的一种辅助手段,对患者体重管理的影响。该试验中,主要终点是在56周时体重指数(BMI)标准差评分(SDS)较基线水平的变化[4]。
数据显示,与安慰剂相比,在使用Saxenda作为生活方式治疗的辅助手段时,肥胖症青少年患者的BMI-SDS、BMI、平均体重和其他体重相关终点均显著降低。在青少年人群中观察到的不良事件与在成人中观察到的相似。最常见的不良反应是胃肠道事件,包括恶心、呕吐和腹泻。
3
利拉鲁肽未来市场前景
市场常胜将军——利拉鲁肽
利拉鲁肽虽然上市较晚,但凭借其独特的疗效优势,一跃成为“降糖新宠”。利拉鲁肽上市当年即获 GLP-1类药物销售冠军,成为最畅销的GLP-1受体激动剂。在2019年全球降糖药销售额排行榜中,利拉鲁肽以36.3亿美元成为全球第二畅销的降糖药。此外,利拉鲁肽另一适应症也于2014年年底经FDA获批上市,成为唯一一个用于减肥的针剂,2019年用于减肥的销售额达13亿美元,同比增幅达123%。
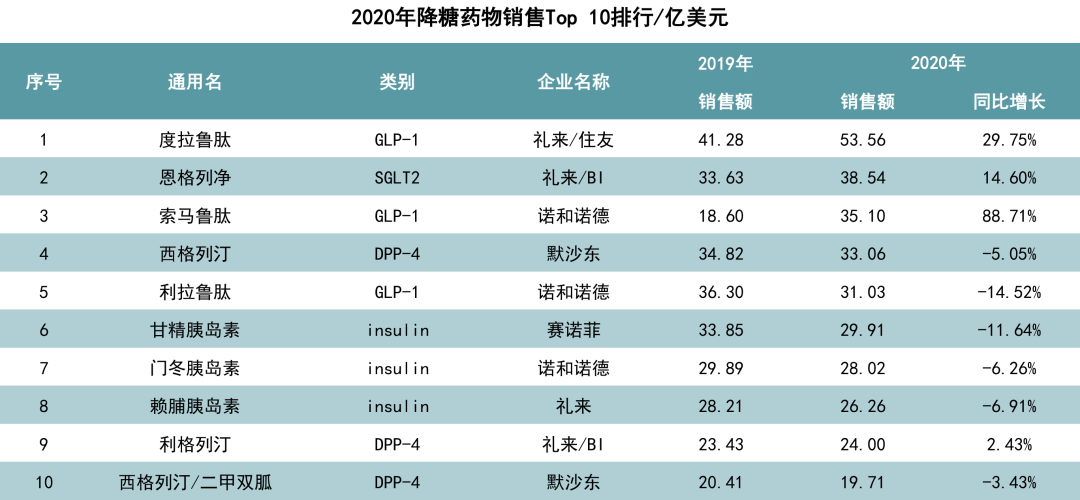
2020年降糖药物销售Top 10排行/亿美元[5]
上市后的前几年,由于价格原因,诺和力销售情况并不理想。但自从2017年进入医保,诺和力开始逐渐放量,2019年至2021年国内销售额逐年增长,分别为8.98、10.33、15.44亿丹麦克朗,与其在全球销售额的负增长局面相反。由于同类降糖药以及其他作用机制降糖药的竞争,2019年利拉鲁肽全球销售额开始下降,并被Eli Lilly的长效GLP-1类似物度拉糖肽反超。2021年利拉鲁肽全球销售额下降20%至23亿美元。不过,未来随着新适应症的获批,利拉鲁肽有望进一步迎来销售额新高。
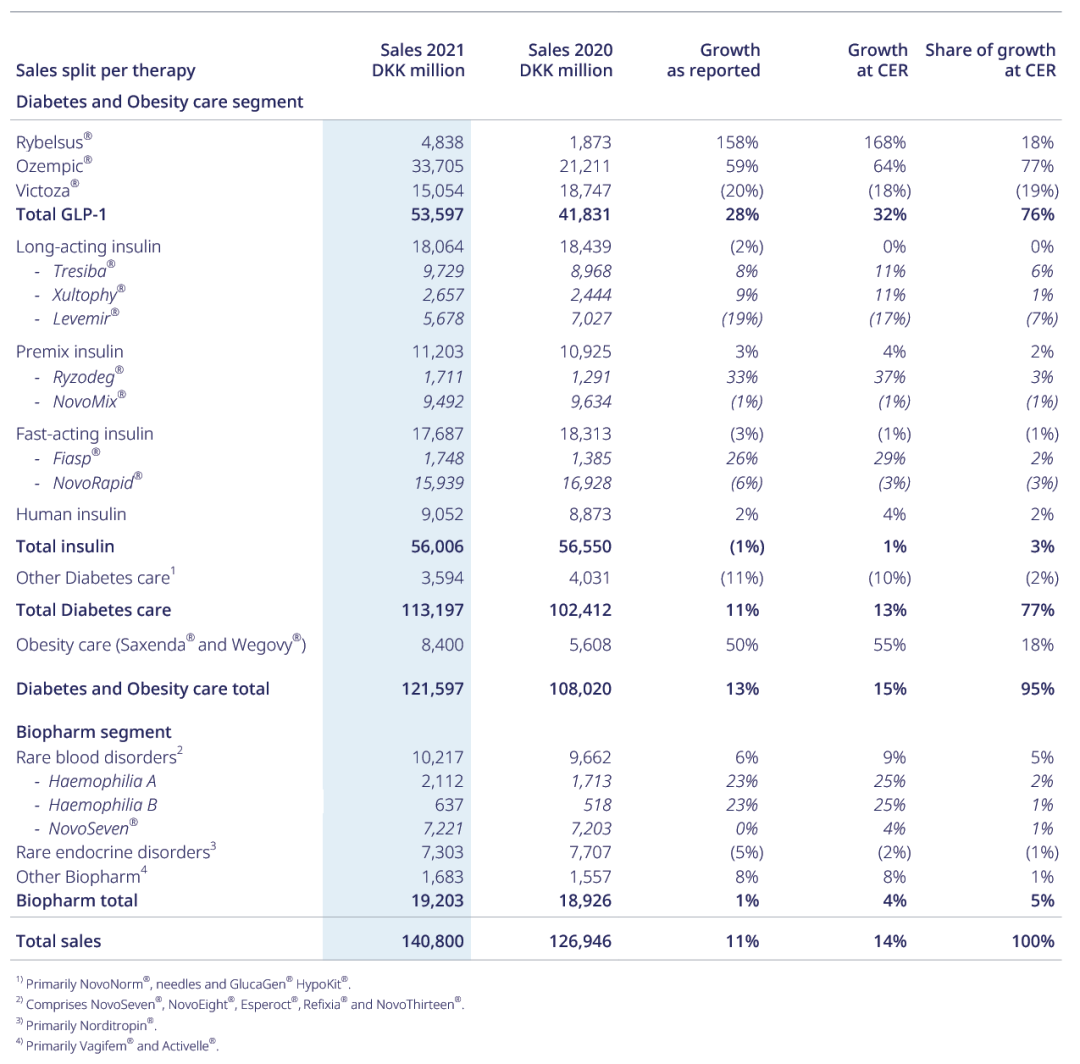
Novo Nordisk2021财年表现[6]
此外,利拉鲁肽于2017年被纳入国家医保谈判乙类目录,价格由723元/支降至410元/支(3ml:18mg),降幅达43%,成为国内首个纳入医保的GLP-1激动剂。作为最有前景的新型降糖药,利拉鲁肽在控糖有效性、安全性和药物经济学方面均颇有优势,进入医保目录这无疑是广大糖尿病患者的福音。
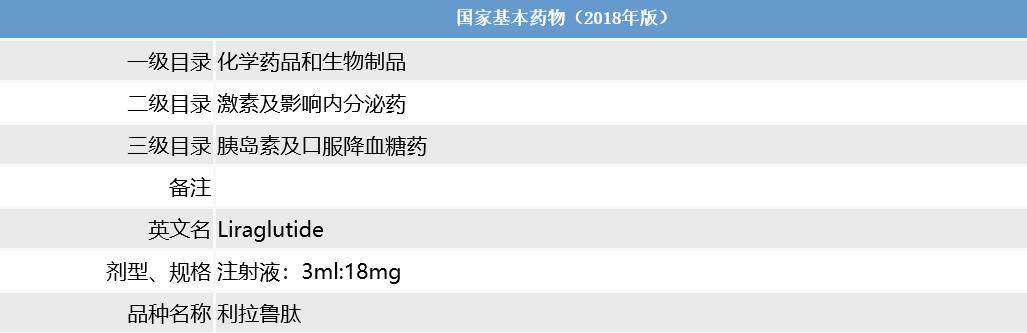
利拉鲁肽被纳入国家医保名录
(来源:http://app1.nmpa.gov.cn/)
利拉鲁肽市场未来展望
鉴于利拉鲁肽的特殊功效,现今许多国内外指南或共识(如加拿大糖尿病指南、《2型糖尿病合并动脉粥样硬化性心血管疾病降糖药物应用中国专家共识》)推荐,合并心血管疾病的2型糖尿病患者可优先选择利拉鲁肽。
然而,随着临床研究证据的不断积累以及药物经济性和可及性的改善,早期应用利拉鲁肽(如在新诊断2型糖尿病患者中)也有可能得到较好获益。
利拉鲁肽的主要优势在于降糖平稳、效果较好,可避免其他药物可能引起的体重增加、其他脏器损害及低血糖风险,真正实现了鱼与熊掌兼得,是很多其他降糖药无法比拟的。未来,期待利拉鲁肽能在临床得到更多的应用,使更多患者获益。
目前市场上有两种利拉鲁肽注射液产品,占市场份额超过60%,分别是Victoza和Saxenda。前者以改善血糖控制和减少并发症而闻名,后者通常用于患有健康问题和肥胖的患者。随着近年来患糖尿病、肥胖症的人数不断增加,预计全球利拉鲁肽市场将在2022-2026年预测期内出现大幅增长。
4
湃肽 高技术壁垒的多肽合成研发平台
浙江湃肽生物股份有限公司是一家致力于多肽产业化的国家高新技术企业,拥有全球领先的全固相合成多肽生产与开发工艺,专注于高技术壁垒的多肽原料药研发及生产;拥有超强研发技术团队,已成功研制多个多肽原料药,攻克了在合成端的技术壁垒和价格壁垒。凭借在多肽领域的研发优势、过硬产品质量,获得国内、国际市场较高认可。同时,湃肽一直坚持匠心筑梦,品质为先,力争打造中国多肽领导品牌,持续为客户提供更优质的产品和更专业的服务。

目前公司的利拉鲁肽已完成中美双报,最大单杂0.1%,可批量公斤级生产,此外,湃肽具备丰富的多肽合成和生产经验,可以为客户提供高效率和最大化产能的服务。
作为新一代具有降糖、减重、改善心血管等多重作用的降糖药物,利拉鲁肽在糖尿病及肥胖症治疗的广阔市场,国内多家药企正积极研发报批该产品。站在市场刚刚起步的节点,湃肽将凭借自身优势,抢跑GLP-1领域,快速占据国内外市场份额。
参考文献:
[1]Andersen A, Lund A, Knop FK, Vilsbøll T. Glucagon-like peptide 1 in health and disease. Nat Rev Endocrinol 2018 Jul,14(7):390-403.
[2]杨文英,刘晓民,马建华,et al.利拉鲁肽与格列美脲联合二甲双胍对2型糖尿病的疗效和安全性比较.中华糖尿病杂志. 2011,(06).
[3]Steven P. Marso,Gilbert H,Kirstine Brown-Frandsen,et al.Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes.N Engl J Med 2016 Jul 28,375(4):311-22.
[4]News provided by Novo Nordisk:FDA approves Saxenda® for the treatment of obesity in adolescents aged 12-17.
[5]药春秋.降糖药Top 10榜单公布,GLP-1、DPP-4潜力十足!
[6]https://www.novonordisk.com
[7]凡人股事.从利拉鲁肽看多肽厂家.

扫码关注我们
解锁更多资讯