抗肿瘤利器-肢端肥大症治疗药兰瑞肽
肢端肥大症是一种由垂体前叶过度分泌生长激素(GH)引起的罕见疾病,患者通常因GH和胰岛素样生长因子-1(IGF-1)分泌过多而导致身体结构改变和内分泌代谢紊乱,生活质量和寿命受到严重影响。以兰瑞肽为代表的生长抑素类似物(SSA)可有效抑制GH分泌、缩小肿瘤体积,明显改善患者的生活质量,是肢端肥大症药物治疗的首选。

关于兰瑞肽
兰瑞肽是什么
兰瑞肽(Lanreotide,商品名Somatuline®)是一种用于治疗肢端肥大症以及神经内分泌肿瘤引发的综合征(特别是针对类癌瘤综合征)的药物。它与奥曲肽类似,是长效的生长激素抑制素八肽类似物。
目前,兰瑞肽有两种剂型:一种缓释微球粉针,10-14天进行一次肌肉注射,有30mg和40mg规格;另一种为长效水凝胶注射剂,为一次性注射笔与药品的药械组合,每个月给药一次有60mg/0.2ml,90mg/0.3ml,120mg/0.5ml。

兰瑞肽结构及作用机理
兰瑞肽是首个缓释长效的生长抑素八肽类似物,由1对位于半胱氨酸和半胱氨酸之间的二硫键环化而得,与腺垂体细胞上的生长抑素受体结合力强于奥曲肽。研究表明,兰瑞肽主要通过生长抑素受体-2(SSTR2)和生长抑素受体-5(SSTR5)发挥作用,对外周生长抑素受体的亲和力较强,而对中枢受体的亲和力较弱。
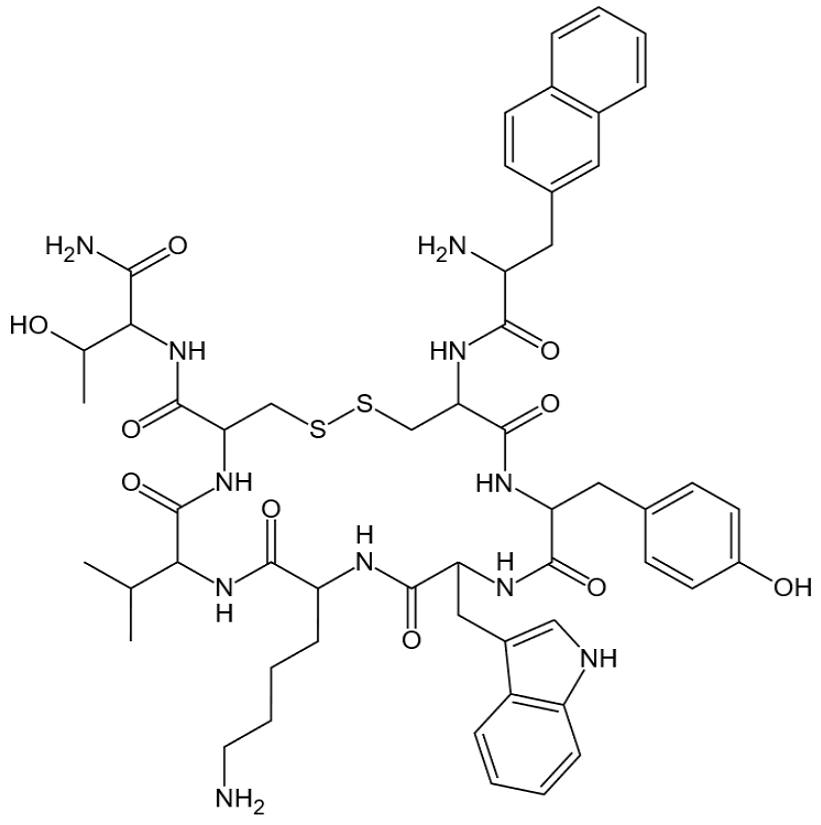
兰瑞肽结构式
兰瑞肽在生长激素分泌和消化道激素分泌方面具有良好的特异作用,较天然生长抑素更具活性,且作用时间更长。同时,其对生长激素分泌的抑制作用较对胰岛素分泌的抑制作用具有明显的选择性,对肠道外分泌、消化道激素和细胞增殖机制有抑制作用。
兰瑞肽市场应用
最初上市的兰瑞肽是以聚合物微球为基础的长效剂型,即注射用醋酸兰瑞肽为主要应用剂型,该剂型采用了无菌冻干的制剂方法,每7天、10天或14天肌肉注射一次,用于肢端肥大症治疗。
为了更好地服务患者,进一步提高患者依从性和提升治疗结局,同时也为了消除在微球制剂的生产过程中所使用的有机溶剂对环境的影响,之后又开发了新一代预充式的水凝胶剂型,即醋酸兰瑞肽缓释注射液(预充式)(索马杜林®ATG),于2001年首先在英国获批并成功投放市场,获得了医生与患者的充分肯定。

索马杜林®ATG
醋酸兰瑞肽缓释注射液(预充式)为水溶性兰瑞肽,采用先进的纳米技术制剂,工艺独特,柔性纳米管形成的液晶状凝胶溶液,是首个基于自组装纳米管技术的生长抑素类似物的缓释制剂。
纳米药物具有独特的优势,即改善药物疗效,可延长给药间隔,降低给药频率,同时提供最大的药理学效应和最小的系统副作用,从而带来更好的临床治疗效果和治疗依从性。正是基于这种先进的纳米技术,多项临床试验已证实醋酸兰瑞肽缓释注射液(预充式)可快速起效,120mg平均达峰时间1.1天;持久释放,给药间隔可从28天最长延长至56天,有助于提高患者的长期治疗依从性,提升生活质量,降低用药负担。
目前兰瑞肽ATG也已被纳入国家医保,且兰瑞肽ATG的90mg和120mg两个剂型的单支价格都比奥曲肽微球便宜,减轻患者经济负担,性价比更高。
兰瑞肽的临床应用
1
用于类癌的对症治疗;
2
肢端肥大症,尤其适用于经外科手术和(或)放射治疗后生长激素分泌异常时;
3
促甲状腺素(TSH)分泌型垂体腺瘤(国外资料);
4
也用于其它类型肿瘤,如绝经后的乳腺癌、神经内分泌肿瘤、直肠癌等(国外资料)。
肢端肥大症治疗[1]
对于兰瑞肽ATG对肢端肥大症的治疗效果,我们可从Pituitary杂志2010年发表的一项研究中略窥一斑,该研究为“醋酸兰瑞肽缓释注射液(预充式)可快速和持续降低肢端肥大症患者的血清GH和IGF-1水平:一项为其52周的多中心、随机、安慰剂对照临床研究”,共纳入了来自8个国家、30个治疗中心的108例患者。
该研究的方案设计为兰瑞肽ATG每28天皮下注射一次,共注射13次,分为四个阶段:①洗脱阶段,即对先前接受过SRLs或多巴胺受体激动剂(DA)治疗的患者进行停药洗脱;②双盲治疗阶段,患者分别应用60、90或120 mg单次剂量的兰瑞肽ATG并与安慰剂组进行双盲比较;③单盲治疗阶段,应用以上固定剂量进行三次注射;④开放标签阶段,根据生化反应在第五次和第八次治疗时调整用药剂量和间隔。同时,分别在第4、13、14、15、16、32和52周测定患者血清中GH和IGF-1的水平。主要疗效终点为从基线到第4周平均GH水平下降>50%的患者比例。本项研究入组标准为:年龄≥18岁的肢端肥大症患者;从未接受过SSA或DA治疗,或在入组3个月前停止服用以上药物的患者,平均血清GH水平在筛查时>5 ng/ml。最终,研究共入组了108例患者,其中99例完成了52周的治疗。
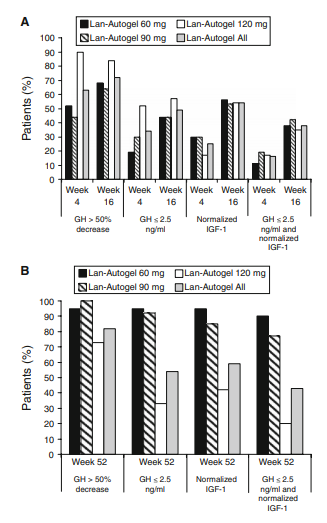
控制生长激素 (GH) 和胰岛素样生长因子-1 (IGF-1) A 在第 4 周和第 16 周按随机给药的剂量和 B 在第 52 周按最后一次给药的患者的比例
结果显示,在肢端肥大症的常见症状改善方面,在治疗16周后与基线相比,超过90%的患者的多汗、头痛、乏力、关节疼痛等症状都有缓解或稳定,并且症状的控制和改善在治疗52周后仍可保持。整体体现了兰瑞肽ATG能够快速降低、持续改善肢端肥大症患者生化指标,生化指标和临床症状缓解率高的特点。
在安全性方面,兰瑞肽ATG治疗组患者总体耐受性良好,不良事件发生率低。108例入组患者中有99例完成了治疗方案,未有因治疗相关不良事件而停药的情况发生。最常见的不良反应为胃肠道反应,心脏事件的发生率并不高,且发生情况可预期。深部皮下注射兰瑞肽ATG对免疫原性的影响可忽略不计。
胃肠胰神经内分泌肿瘤治疗[2]
2014年,NEJM上公布了一项研究,探讨了兰瑞肽对胃肠胰神经内分泌肿瘤患者PFS的影响。
该研究为一项随机、双盲、安慰剂对照的多国研究,探讨生长抑素类似物兰瑞肽的疗效,研究对象为晚期、分化良好或中度分化、无功能、生长抑素受体阳性的神经内分泌肿瘤患者,分级为1或2级(Ki67增殖指数<10%)。肿瘤起源于胰腺、中肠,后肠或不明来源。
患者随机分配接受120mg的兰瑞肽缓释水凝胶制剂(Autogel)(n=101)或者安慰剂(n=103),每28天一次,持续96周。主要终点是无进展生存期(PFS),次要终点包括总生存期、生活质量和安全性。
主要研究结果
大多数患者(96%)在分组前3-6月内无肿瘤进展,33%患者肝肿瘤体积大于25%。兰瑞肽相比于安慰剂可明显延长PFS(中位未达到 vs 18.0个月,p<0.001)(下图)。24个月预计无进展生存率,兰瑞肽和安慰剂组分别为65.1%(95%CI,54.0-74.1)和33.0%(95%CI,23.0-43.3)。预定的亚组人群的治疗效应与总人群一致。两组间在生活质量或者总生存方面没有差异。
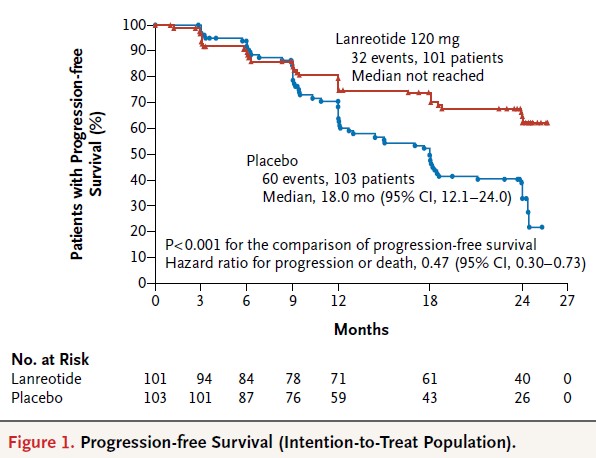
最常见的治疗相关不良事件是腹泻(兰瑞肽和安慰剂分别为26%和9%)。
结论
兰瑞肽可显著延长转移性胃肠胰神经内分泌肿瘤(Ki-67<10%)的PFS。
兰瑞肽未来市场前景
兰瑞肽市场需求旺盛 潜力巨大
根据美国神经外科医生协会的数据,库欣病每年影响大约1000万到1500万人。此外,该病主要影响20至50岁的人群,女性患病率高于男性。此外,根据2018年NCBI的数据,全球肢端肥大症患病率约为每百万人4600例。在全世界,每年每百万人中约有116.9例新发肢端肥大症。因此,这种罕见疾病发病率的上升是全球Lanreotide市场的推动因素。
推动整个市场增长的另一个重要因素是,为罕见疾病患者提供有吸引力的政府保险计划和项目。例如,美国和欧洲的一些政府医疗机构,如美国国立卫生研究院(NIH)和国家推进转化科学中心(NCATS),为罕见疾病提供补贴药物。

未来,随着肢端肥大症的高患病率,以及公众对如何治疗这种罕见疾病的认识的提高,有望促进全球Somatuline市场的发展。有调研机构预测,全球Somatuline的市场规模在2022-2026年预测期内将以4.2%年复合增值率增长,市场前景不可限量。
湃肽 高技术壁垒的多肽合成研发平台
浙江湃肽生物股份有限公司是一家致力于多肽产业化的国家高新技术企业,拥有全球领先的全固相合成多肽生产与开发工艺,专注于高技术壁垒的多肽原料药研发及生产;拥有超强研发技术团队,已成功研制多个多肽原料药,攻克了在合成端的技术壁垒和价格壁垒。凭借在多肽领域的研发优势、过硬产品质量,获得国内、国际市场较高认可。同时,湃肽一直坚持匠心筑梦,品质为先,力争打造中国多肽领导品牌,持续为客户提供更优质的产品和更专业的服务。

未来,湃肽将抓住多肽类仿制药市场高速增长的发展机遇,继续深耕多肽类药物市场,提升工艺技术、研发实力,持续增强市场竞争力和产品的硬实力。同时,公司还将积极布局多肽创新药业务领域,推动多肽创新药市场发展繁荣,让多肽药得以低成本惠及全球患者,造福人类健康。
参考文献:
[1]Shlomo Melmed,David Cook,Jochen Schopohl,et al.Rapid and sustained reduction of serum growth hormone and insulin-like growth factor-1 in patients with acromegaly receiving lanreotide Autogel therapy: a randomized, placebo-controlled, multicenter study with a 52 week open extension.Randomized Controlled Trial Pituitary 2010,13(1):18-28.
[2]M. Caplin,P. Ruszniewski,M. Pavel,et al.Progression-free survival (PFS) with lanreotide autogel/depot (LAN) in enteropancreatic NETs patients: The CLARINET extension study.Journal of Clinical Oncology 32(15_suppl):4107-4107.

扫码关注我们
解锁更多资讯